Согласно основному уравнению молекулярно-кинетической теории, давление р прямо пропорционально средней кинетической энергии и  поступательного движения молекул:
поступательного движения молекул:

где n — объемная концентрация молекул. Заменив в  n отношением числа молекул N к объему газа
n отношением числа молекул N к объему газа  получим:
получим:
 .
.
В состоянии теплового равновесия при постоянном объеме средняя кинетическая энергия данной массы газа должна иметь вполне определенное значение, как и температура. Согласно формуле  , это означает, что отношение
, это означает, что отношение  для данной температуры должно быть одним и тем же для любых идеальных газов. То, что это действительно так, было подтверждено экспериментально для разных газов, находящихся в условиях теплового равновесия при постоянном объеме (измерялось давление).
для данной температуры должно быть одним и тем же для любых идеальных газов. То, что это действительно так, было подтверждено экспериментально для разных газов, находящихся в условиях теплового равновесия при постоянном объеме (измерялось давление).
Абсолютная температура .
Таким образом, величина  которую, в отличие от микропараметра
которую, в отличие от микропараметра  , легко измерить, является вполне однозначной характеристикой теплового состояния газа, как и температура. Измеряется
, легко измерить, является вполне однозначной характеристикой теплового состояния газа, как и температура. Измеряется  (как и энергия) и джоулях. Зависит она только от температуры и может рассматриваться как естественная мера температуры. Однако в силу укоренившейся привычки измерять температуру в градусах был введен коэффициент пропорциональности k между температурой
(как и энергия) и джоулях. Зависит она только от температуры и может рассматриваться как естественная мера температуры. Однако в силу укоренившейся привычки измерять температуру в градусах был введен коэффициент пропорциональности k между температурой  , выраженной в энергетических единицах, и температурой T, выраженной в градусах:
, выраженной в энергетических единицах, и температурой T, выраженной в градусах:
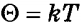 ,
,
или
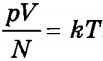 .
.
Температура T , определяемая равенством , называется абсолютной температурой .
Абсолютный нуль температуры .
Значения температуры, определенной по формуле  , всегда положительны в силу положительности
, всегда положительны в силу положительности  (ни давление, ни объем, ни число частиц отрицательными быть не могут).
(ни давление, ни объем, ни число частиц отрицательными быть не могут).
Поэтому минимальным значением температуры является нуль. Температура может равняться нулю, если давление либо объем равны нулю. Из принятого определения температуры следует, что нулем температуры является температура, при которой прекращается хаотическое движение молекул. Она называется абсолютным нулем температуры.
Температура, как и давление, определяется средней кинетической энергией молекул идеального газа. Поэтому температура, как и давление, является статистической величиной (статистической называется величина, имеющая смысл только для систем, содержащих очень большое число частиц). Нельзя говорить о температуре одной или нескольких молекул.
Абсолютную шкалу температур ввел английский ученый У. Кельвин в 1860 г. Нулевая температура по абсолютной шкале (ее называют также шкалой Кельвина) соответствует абсолютному пулю, а каждая единица температуры по этой шкале равна градусу по шкале Цельсия.
Единица абсолютной температуры является одной из семи основных единиц СИ и измеряется в Кельвинах (обозначается буквой К).
Связь между температурами, измеренными по шкалам Цельсия t и Кельвина Т. описывается формулой:
 .
.
Абсолютный нуль равен -273.15 ºС. Как правило, при расчетах пользуются округленным значением абсолютного нуля (-273 ºС).
Постоянная Больцмана .
Коэффициент пропорциональности k в формуле называется постоянной Больцмана в честь Л. Больцмана, одного из основателей молекулярно-кинетической теории газа. Этот коэффициент составляет k = 1,38 -23 Дж/К.
Постоянная Больцмана связывает температуру  в энергетических единицах с температурой T в кельвинах. Это одна из наиболее важных постоянных в молекулярно-кинетической теории.
в энергетических единицах с температурой T в кельвинах. Это одна из наиболее важных постоянных в молекулярно-кинетической теории.
 Электромагнитные колебания
Электромагнитные колебания


