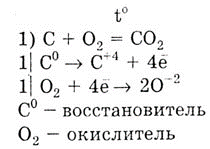В IV группе (подгруппе углерода) стоят следующие химические элементы:
- углерод (С),
- кремний (Si),
- германий (Ge),
- олово (Sn),
- свинец (Pb).
В группе сверху вниз увеличивается порядковый номер атомов, а соответственно, растет число оболочек - атомный радиус. Неметаллические свойства (окислительные) ослабевают, а металлические (восстановительные) – усиливаются (углерод и кремний – неметаллы, а свинец, олово, германий – металлы).
Степень окисления может быть различной: -4, 0, +2, +4.
Высшие оксиды подгруппы углерода (СО2, SiО2) имеют кислотный характер, оксиды остальных элементов подгруппы - амфотерны (GeО2, SnО2, PbО2), вследствие чего они могут реагировать с кислотными и с основными соединениями.
Кислоты (H2ЭлO3), образованные этими элементами слабые.
Водородные соединения: СН4; SiH4, GeH4. SnH4, PbH4.
Углерод и кремний - это неметаллы, на внешнем энергетическом уровне находятся 4 неспаренных электрона. У кремния радиус больше, поэтому восстановительная способность у него выше. Углерод — восстановитель: