Закон Авогадро состава сформулирован в 1811 г итальянский химик Амедео Авогадро.
Закон Авогадро формулируется так:
В равных объёмах любых газов, взятых при одной и той же температуре и при одном и том же давлении, содержится одно и то же число молекул.
Следствие из закона:
1 моль (6,02×1023 молекул – число Авогадро) любого газа при нормальных условиях занимает объем 22,4 л. Эта величина называется молярный объём.
Vm = 22,4 л,
Нормальными условиями (н.у.) считают температуру 0оС (273 K) и давление 1 атм (760 мм ртутного столба или 101 325 Па).
Пример. Определить число молекул, содержащихся в воде количеством 0,5 моль.
N(H2O) = NA·× ν(H2O) = 6,02·× 1023 моль-1·× 0,5 моль = 3,01·× 1023.
Молекулярная масса Mr – отношение массы молекулы к 1/12 части массы атома углерода С.
Молярная масса M – отношение массы вещества m к его количеству ν, выражается в единицах г/моль.
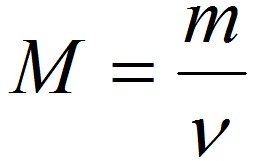 ,
,
Из закона Авогадро следует, что массы двух газов (m1 и m2), взятых в одинаковых объёмах, должны относится друг к другу, как их как их молекулярные массы или как численно равные их молярные массы (M1 и M2):
 .
.
Отношение массы одного газа к массе другого газа, взятого при тех же условиях (температуре и давлении), называется относительной плотностью первого газа по второму.
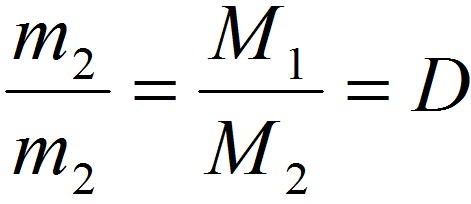 ,
,
откуда
М1=DM2.
Взаимосвязь молярной массы, молярного объёма, числа Авогадро и количества вещества:
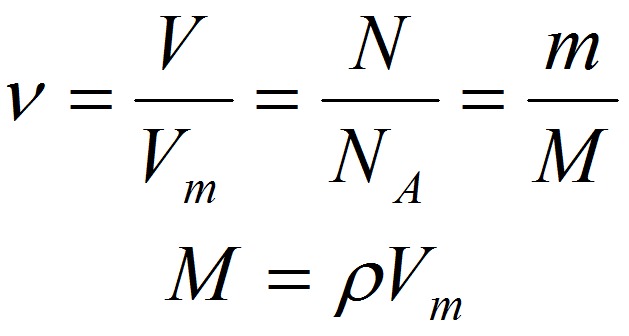 ,
,
Для приведения объёма газа к нормальным условиям используется уравнение, объединяющее законы Бойля-Мариотта и Гей-Люссака:
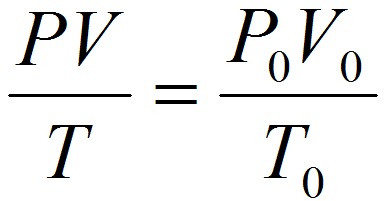 ,
,
где V – объём газа при давлении Р и температуре Т.
Молярные массы можно вычислить пользуясь уравнением Менделеева-Клапейрона:
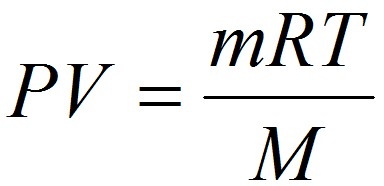 ,
,
где:
Р – давление газа, Па;
V – объём газа, м3;
m – масса вещества, г;
М – молярная масса вещества;
Т – абсолютная температура;
R – универсальная газовая постоянная 8,314 Дж/(моль×К).
Пример. Какой объём занимает 0,2 моль N2 при н.у.?
|
Дано: Vm = 22,4 л/моль ν(N2) = 0,2 моль Найти: V(N2) |
Решение: 1. Используем формулу
откуда
Ответ: V(N2) = 4,48 л. |

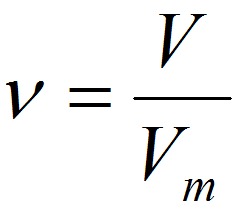 ,
,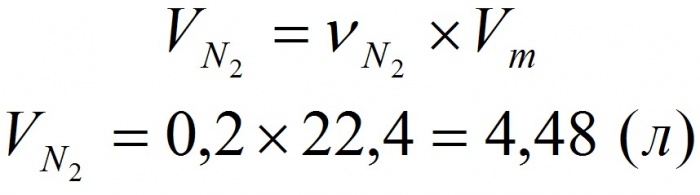 ,
,